Бензол. Химические свойства. Химические свойства бензола Реакции взаимодействия бензола
Бензольное ядро довольно устойчиво. Оно более склонно к реакциям замещения атомов водорода бензольного кольца, нежели к реакциям присоединения по месту разрыва двойных связей. В этом выражении его «ароматический характер».
Реакции замещения
Наиболее характерны реакции электрофильного замещения: нитрирование, сульфирование, алкилирование (ацилирование), галогенирование (галогенирование гомологов бензола может идти и по радикальному механизму.
1. Нитрование - замещение водорода бензольного кольца нитрогруппой - проводят так называемой нитрирующей смесью - смесью концентрированных азотной и серной кислот. Действующим агентом является катион нитрония N0 2 + :
НО - N0 2 + 2H 2 S0 4 →N0 2 + + 2HS0 4 - + H 3 0
Нитроний катион гидроксоний катион
Механизм нитрования (как и всех реакций замещения) следующий:
Присутствие воды в реакционной смеси мешает течению реакции, т.к. вода участвует в процессе, обратном образованию катиона нитрония. Поэтому для связывания выделяющейся в реакции воды берут избыток концентрированной серной кислоты.
Правила замещения водородов бензольного ядра. Если в бензольном ядре имеется какой-нибудь заместитель водорода, то в реакциях электрофильного замещения он играет роль ориентанта - реакция идет преимущественно в орто- и пара-положения по отношению к заместителю (ориентант I рода) или в мета-положения (ориентант II рода).
Заместители I рода направляют атакующий электрофил в орто- и пара-положения по отношению к себе. Приводим их в порядке убывания ориентирующей силы (электродонорного эффекта):
Заместители II рода направляют атакующий электрофил в мета-положения по отношению к себе. Приводим их также в порядке убывания ориентирующей силы:
Например, -ОН - группа - ориентант I рода:


59. Напишите уравнение и механизм реакций нитрования следующих соединений: а) бензол; б) толуол; в) хлорбензол; г) нитробензол; д) сульфобензол; е) цианистый фенил; ж) метоксибензол; з) аминобензол.

Заместители I рода являются электродонорными, они увеличивают плотность электронного облака бензольного ядра, особенно в орто- и пара-положениях и тем самым (облегчают) активируют бензольное ядро к атаке электрофила. Однако σ-комплекс (III) стабилизируется не присоединением аниона, а отщеплением катиона водорода (энергия, выделяющаяся при образовании единого π-электронного облака бензольного ядра, 36,6 ккал/моль):

Заместители II рода являются электроноакцепторными, они как бы оттягивают на себя часть электронного облака, тем самым уменьшают плотность электронного облака бензольного ядра, особенно в орто- и пара-положениях по отношению к себе. Заместители II рода в общем-то затрудняют реакции электрофильного замещения. Но в мета-положениях по отношению к заместителю II рода плотность облака несколько выше, чем в других. Поэтому реакции электрофильного замещения в случае заместителей II рода идут в мета-положения:
 |

Описанные выше правила не носят характера законов. Речь почти всегда идет только о главном направлении реакции. Например, при нитровании толуола образуется 62 % орто-, 33,5 % пара- и 4,5 % мета-нитротолуолов.
Довольно сильное влияние на направления реакций оказывают условия проведения (температура, присутствие катализаторов и др.).
При наличии двух ориентантов в бензольном ядре возможна согласованная и несогласованная ориентация этих двух заместителей. В случае несогласованной ориентации заместителей одного рода направление реакции определяет более сильный (см. ряды заместителей I и II рода):

В случае несогласованной ориентации заместителей разного типа направление реакции определяет заместитель I рода, так как он активирует бензольное ядро к электрофильной атаке, например,

60. Согласно правилам замещения, напишите нитрование следующих двузамещенных бензола: а) м-нитротолуола; б) п-нитротолуола; в) о-окситолуола; г) п-хлортолуола; д) м-нитробензойной кислоты; е) п-оксихлорбензола; ж) м-хлортолуола; з) п-метокситолуола.
2. Реакция сульфирования протекает при нагревании аренов с концентрированной серной кислотой или олеумом. Атакующим агентом является молекула SO 3 , играющая роль электрофила:

Первая стадия сульфирования - медленная, реакция в целом обратимая:

Сульфокислоты по силе сравнимы с минеральными, поэтому в водных растворах они находятся в ионизированном состоянии (III).
61. Приведите уравнения и механизмы реакций сульфирования следующих веществ, придерживаясь правил замещения:
а) толуола; б) о-ксилола; в) нитробензола; г) о-нитротолуола; д) п-хлорнитробензола; е) м-нитротолуола; ж) п-аминотолуола; з) о метокситолуола.
3. Реакция галогенирования
аренов на холод в присутствии катализаторов типа AlCl 3 , AlBr 3 , FeCl 3 - типичная электрофильная реакция, ибо катализаторы способствуют поляризации связи в молекуле галогена (вплоть до ее разрыва): 
Таким же образом действует и безводное хлорное железо:

В условиях радикальной реакции (свет, нагревание) галогены (хлор, бром) замещают водороды боковых цепей (аналогично галогенированию алканов):

В более жестких условиях происходит и радикальное присоединение галогенов к ароматическому ядру.
62 . Напишите уравнения и механизмы реакции и назовите продукты:
а) толуол + хлор (при ярком свете и нагревании);
б) толуол + хлор (на холоду в присутствии катализатора);
в) нитробензол + хлор (на холоду в присутствии катализатора);
г) п-нитротолуол + хлор (при ярком свете и нагревании);
д) п-нитротолуол + хлор (на холоду в присутствии катализатора):
е) этилбензол + хлор (при ярком свете и нагревании);
ж) этилбензол + хлор (на холоду в присутствии катализатора);
з) п-окситолуол + хлор (на холоду в присутствии катализатора);
и) м-нитротолуол + хлор (на холоду в присутствии катализатора);
к) м-ксилол + хлор (на холоду в присутствии катализатора).
4. Алкилирование аренов. В присутствии безводного AlCl 3 (А1Вrз) галогеналканы алкилируют бензол, еще легче, чем его гомологи, а также их галогенпроизводные (реакции Густавсона-Фриделя-Крафтса). Катализатор, образуя комплекс А1Сl 3 , поляризует связь С-Гал вплоть до разрыва ее, и поэтому атакующий агент-электрофил:

Алкилирование алкенами в присутствии А1Сl 3 , BF 3 или Н 3 РО 4 приводит к аналогичным результатам (механизм тоже электрофильный):


Алкилирование галогеналканами и алкенами как электрофильные реакции идут в соответствии с правилами замещения водородов бензольного кольца. Однако процесс осложняется дальнейшим алкилированием продуктов реакции и другими нежелательными явлениями. Чтобы последние свести к минимуму, реакцию ведут при возможно низкой температуре, оптимальном количестве катализатора и большом избытке арена.
63. Приведите уравнения и механизм реакций в условиях Густавсона-Фриделя-Крафтса между следующими веществами:
а) бензол + 2-хлорпропан; б) бензол + 2-хлор-2-мегилпропан; в) бензол + бензилхлорид; г) бромбензол + бромэтан; д) толуол + бутилхлорид; е) толуол + бромэтан; и) п-бромтолуол + изопропилбромид; з) м-бромтолуол + бромэтан; и) п-бромтолуол + изопропилбромид; к) хлорбензол + бензилхлорид.
64. Напишите уравнения реакций алкилирования аренов алкенами в присутствии фосфорной кислоты, приведите механизм:
а) бензол + этилен; б) бензол + пропилен; в) толуол + этилен; г) толуол + пропилен; д) бензол + изобутилен; е) толуол + изобутилен; ж) м-ксилол + этилен; з) п-ксилол + этилен.
5. Реакция окисления (определение числа боковых цепей). Ароматическое ядро очень устойчиво к окислителям. Так, бензол и его гомологи не реагируют с перманганатом калия подобно алканам. В этом тоже выражается их «ароматический характер». Но при нагревании гомологов бензола с окислителями в жестких условиях бензольное ядро не окисляется, а все боковые углеводородные цепи, независимо от их длины, окисляются до карбоксильных групп, продуктами окисления являются ароматические кислоты. По количеству карбоксильных групп в последних судят о числе боковых цепей в исходном гомологе бензола 1 .

65 . Напишите уравнения реакций окисления следующих веществ: а) этилбензол; б) о-диметилбензол; в) пропилбензол; г) рядовой триметилбензол; д) п-метилизопропилбензол; е) о-нитротолуол; ж) 3-нитро-1-метил-4-этилбензол; з) симметричный триметилбензол.
6. Реакции присоединения. Хотя ароматическое ядро менее склонно к реакциям присоединения, чем замещения, в некоторых условиях они имеют место. Особенностью реакций присоединения является то, что к одному молю бензола (или его гомолога) всегда присоединяется по три моля галогена, водорода, озона, что объясняется наличием у ароматического ядра единого π-электронного облака с определенной единой, общей энергией трех двойных связей (вернее, шести π-электронов).
а) Гидрирование идет в присутствии катализаторов (Pt, Pd и др.) при 110°С (Н.Д. Зелинский и др.).

б) Галогенирование идет при пропускании паров брома или хлора через кипящий бензол под действием прямого солнечного света или при освещении УФ-лучами (кварцевая лампа):

в) Озонирование. Подобно алкенам ароматические углеводороды легко подвергаются озонолизу.

66. Напишите уравнения реакций присоединения (гидрирования, галогенирования при освещении УФ-лучами, озонирования) со следующими аренами: а) толуол; б) о-ксилол; в) м-ксилол; г) п-ксилол; д) этилбензол; е) о-этилтолуол; ж) м-этилтолуол; з) п-изопропилтолуол. Назовите полученные продукты.
Бензол является ненасыщенным соединением, но мы выяснили, что в его структуре нет двойных связей, а есть ароматическая связь – делокализованное электронное облако. Типичные реакции непредельных углеводородов – электрофильное присоединение и окисление – для бензола не характерны. Так, он не обесцвечивает бромную воду, не даёт реакции Вагнера (окисление раствором перманганата калия при комнатной температуре). Для бензола характерны реакции, не приводящие к нарушению замкнутой сопряжённой системы, – реакции замещения. Чтобы выяснить, какой тип замещения (радикальное, электрофильное, нуклеофильное) характерен для бензола, вспомните его электронное строение: σ-скелет молекулы плоский, а над и под плоскостью расположено ароматическое облако. Чтобы провзаимодействовать с этим ароматическим облаком, реагент должен быть электрофильным. Итак, для бензола (и ароматических соединений вообще) характерны реакции электрофильного замещения . Примерами реакций S E являются:
На первой стадии электрофил подходит к молекуле бензола и взаимодействует со всем ароматическим облаком (они притягиваются друг к другу). Образуется π-комплекс
. Для образования новой ковалентной связи углерод-электрофил необходима пара электронов. Электрофил вырывает её из ароматического облака, образуется σ-комплекс
. Он не является замкнутой сопряжённой системой, т.к. атом углерода, образовавший новую σ-связь, перешёл в sp 3 -гибридизацию (он вышел из плоскости и больше не имеет негибридной p z -орбитали). Остальные пять атомов углерода продолжают участвовать в сопряжении, образуя общее электронное облако, в котором делокализовано четыре электрона (6-2=4), поэтому положительный заряд в σ-комплексе обозначается не на конкретном атоме углерода, а в центре разомкнутого кольца. Итак, σ-комплекс не является ароматической структурой. Для того чтобы вернуть ароматичность, ему необходимо отщепить протон водорода (H +). Его забирает оставшийся в реакционной среде нуклеофил (Nu -). Два электрона связи C-H возвращаются в ароматическое облако, атом углерода вновь становится
sp 2 -гибридизованным и может участвовать в сопряжении.
Лимитирующей стадией реакции электрофильного замещения является стадия образования σ-комплекса, т.к. при этом происходит потеря ароматичности, что требует затрат энергии.
Различные реакции электрофильного замещения в бензоле протекают по общему механизму и отличаются только стадией образования электрофильной частицы.
Реакция нитрования бензола протекает под действием смеси концентрированных азотной и серной кислот (схему реакции см. выше). Рассмотрим её механизм.
 |
На первой стадии реакции азотная кислота взаимодействует с серной. В данном случае азотная кислота выполняет роль основания, принимая протон от молекулы серной кислоты (по теории Бренстеда, кислота – это молекула или ион, отдающие протон, а основание – молекула или ион, принимающие протон водорода). Образуется протонированная азотная кислота, которая, отщепляя молекулу воды, превращается в катион нитрония, или нитроний-катион. Это и есть электрофильная частица. Таким образом, серная кислота выполняет роль катализатора, принимая участие в образовании электрофильного реагента. Вторая роль серной кислоты – это роль водоотнимающего средства. Воду необходимо отводить из сферы реакции, чтобы сместить её равновесие вправо.
После образования электрофила – катиона нитрония - реакция протекает по общему механизму, через образование π- и
σ-комплексов:
Обратите внимание: на стадии превращения σ-комплекса в нитробензол (стадии возвращения ароматичности) протон водорода отщепляется под действием аниона серной кислоты, при этом вновь образуется серная кислота, что доказывает, что она являлась катализатором данной реакции.
 Катализатором реакции галогенирования
являются так называемые кислоты Льюиса (по теории Льюиса, кислоты – это нейтральные молекулы или ионы, способные принимать пару электронов): FeCl 3 , FeBr 3 , AlCl 3 , AlBr 3 и т.п. Катализатор необходим, чтобы поляризовать молекулу галогена. Кислота Льюиса смещает на себя неподелённую электронную пару хлора, образуя комплекс, в котором на одном из атомов хлора сосредоточивается частичный положительный заряд:
Катализатором реакции галогенирования
являются так называемые кислоты Льюиса (по теории Льюиса, кислоты – это нейтральные молекулы или ионы, способные принимать пару электронов): FeCl 3 , FeBr 3 , AlCl 3 , AlBr 3 и т.п. Катализатор необходим, чтобы поляризовать молекулу галогена. Кислота Льюиса смещает на себя неподелённую электронную пару хлора, образуя комплекс, в котором на одном из атомов хлора сосредоточивается частичный положительный заряд:
На стадии образования π-комплекса происходит дальнейшая поляризация связи Cl-Cl, и она разрывается гетеролитически, причём Cl + сразу участвует в образовании σ-комплекса.
 Аналогично протекают реакции алкилирования
(реакция Фриделя-Крафтса).
Аналогично протекают реакции алкилирования
(реакция Фриделя-Крафтса).
 |
Связь C-Cl в метилхлориде недостаточно полярна, чтобы разорваться гетеролитически. Под действием кислоты Льюиса увеличивается частичный положительный заряд на атоме углерода, и комплекс реагента с катализатором является более сильным электрофилом, чем исходный метилхлорид.
Реакция сульфирования бензола протекает под действием олеума (раствор серного ангидрида SO 3 в концентрированной серной кислоте).
Молекула серного ангидрида является электрофилом из-за большого по величине частичного положительного заряда на атоме серы.
 |
При образовании π-комплекса связь S=O (в первую очередь π-связь) поляризуется и разрывается по гетеролитическому типу, поэтому при образовании σ-комплекса на атоме кислорода возникает полный отрицательный заряд. Для восстановления ароматичности протон водорода отщепляется от атома углерода кольца и переходит к отрицательно заряженному кислороду. Образуется бензолсульфокислота.
Когда мы рассматриваем реакции электрофильного замещения в бензоле, перед нами не стоит вопрос, в каком положении протекает реакция, т.к. все атомы углерода абсолютно равноценны. Другое дело, если в бензольном кольце уже есть заместитель. В этом случае в результате электрофильного замещения принципиально возможно образование трёх изомеров:
 |
Чтобы ответить на вопрос, какой из этих возможных продуктов является преобладающим, необходимо рассматривать электронные эффекты заместителя.
Отвлечёмся от реакций электрофильного замещения в бензоле и его производных и рассмотрим электронные эффекты в целом.
Взаимное влияние атомов в молекулах органических
соединений. Электронные эффекты
Атомы и атомные группы в молекулах органических соединений влияют друг на друга, причём не только атомы, непосредственно связанные друг с другом. Это влияние каким-то образом передаётся по молекуле. Передача влияния атомов в молекулах за счёт поляризации связей называетсяэлектронными эффектами . Существует два вида электронных эффектов: индуктивный и мезомерный эффект.
Индуктивный эффект - это передача влияния заместителей по цепи σ-связей за счёт их поляризации. Индуктивный эффект обозначается символом I. Рассмотрим его на примере 1-хлорбутана:
Связь C-Cl полярна из-за более высокой электроотрицательности хлора. На атоме углерода возникает частичный положительный заряд (δ+). Электронная пара следующей σ-связи смещается в сторону электронодефицитного атома углерода, т.е. поляризуется. За счёт этого на следующем атоме углерода также возникает частичный положительный заряд (δ+’) и т.д. Таким образом, хлор индуцирует поляризацию не только «собственной» σ-связи, но и последующих в цепи. Обратите внимание, что каждый последующий частичный положительный заряд по величине меньше предыдущего (δ+>δ+’>δ+’’>δ+’’’), т.е. индуктивный эффект передаётся по цепи с затуханием. Это можно объяснить низкой поляризуемостью σ-связей. Принято считать, что индуктивный эффект распространяется на 3-4 σ-связи. В приведенном примере атом хлора смещает электронную плотность по цепи связей на себя . Такой эффект называют отрицательным индуктивным эффектом и обозначают –I Cl .
Большинство заместителей проявляют отрицательный индутивный эффект, т.к. в их структуре есть атомы, более электроотрицательные, чем водород (индуктивный эффект водорода принят равным нулю). Например: -F, -Cl, -Br, -I, -OH, -NH 2 , -NO 2 ,
-COOH, >C=O .
 |  |
||
Если заместитель смещает электронную плотность по цепи σ-связей от себя , он проявляет положительный индуктивный эффект (+I). Например:

Кислород с полным отрицательным зарядом проявляет положительный индуктивный эффект.
![]()
В молекуле пропена углерод метильной группы sp 3 -гибридизован, а атомы углерода при двойной связи sp 2 -гибридизованы, т.е. более электроотрицательны. Поэтому метильная группа смещает электронную плотность от себя, проявляя положительный индуктивный эффект (+I CH 3) .
Итак, индуктивный эффект может проявляться в любой молекуле, в которой есть разные по электроотрицательности атомы.
Мезомерный эффект – это передача электронного влияния заместителей в сопряжённых системах, посредством поляризации π-связей. Мезомерный эффект передаётся без затухания, т.к. π-связи поляризуются легко. Обратите внимание: мезомерным эффектом обладают только те заместители, которые сами являются частью сопряжённой системы. Например:
Мезомерный эффект может быть как положительный (+М), так и отрицательный (-М).
В молекуле хлорвинила неподелённая электронная пара хлора участвует в p,π-сопряжении, т.е. вклад хлора в сопряжённую систему больше, чем у каждого из атомов углерода. Поэтому хлор проявляет положительный мезомерный эффект.
 Молекула акрилового альдегида – это
Молекула акрилового альдегида – это
π.π-сопряжённая система. Атом кислорода отдаёт в сопряжение один электрон – столько же, как и каждый атом углерода, но при этом электроотрицательность кислорода выше, чем у углерода, поэтому кислород смещает электронную плотность сопряжённой системы на себя, альдегидная группа в целом проявляет отрицательный мезомерный эффект.
Итак, заместители, отдающие в сопряжение два электрона, обладают положительным мезомерным эффектом. К ним относятся:
а) заместители с полным отрицательным зарядом, например, –O - ;
б) заместители, в структуре которых есть атомы с неподелёнными электронными парами на p z -орбитали, например: -NH 2 , -OH,
-F, -Cl, -Br-, -I, -OR (-OCH 3 , -OC 2 H 5).
Заместители, смещающие электронную плотность по сопряжённой системе на себя, проявляют отрицательный мезомерный эффект. К ним относятся заместители, в структуре которых есть двойные связи, например:
 |
Заместитель может проявлять и индуктивный, и мезомерный эффекты одновременно. В некоторых случаях направление этих эффектов совпадает (например, -I и –M), в других – они действуют в противоположных направлениях (например, -I и +M). Как в этих случаях определить общее влияние заместителя на остальную часть молекулы (другими словами, как определить, является данный заместитель электронодонорным или электроноакцепторным)? Заместители, повышающие электронную плотность в остальной части молекулы, называют электронодонорными, а заместители, понижающие электронную плотность в остальной части молекулы, – электроноакцепторными.
Чтобы определить общее влияние заместителя, необходимо сравнить его электронные эффекты по величине. Если преобладает положительный по знаку эффект, заместитель является электронодонорным. Если преобладает отрицательный по знаку эффект, заместитель является электроноакцепторным. Нужно отметить, что, как правило, мезомерный эффект проявляется сильнее, чем индуктивный (из-за большей способности π-связей к поляризации). Однако есть и исключения из этого правила: индуктивный эффект галогенов проявляется сильнее, чем мезомерный.
Рассмотрим конкретные примеры:
В этом соединении аминогруппа является электронодонорным заместителем, т.к. её положительный мезомерный эффект проявляется сильнее, чем отрицательный индуктивный.
 В этом соединении аминогруппа является электроноакцепторным заметителем, т.к. проявляет только отрицательный индуктивный эффект.
В этом соединении аминогруппа является электроноакцепторным заметителем, т.к. проявляет только отрицательный индуктивный эффект.
В молекуле фенола гидроксильная группа является электронодонорным заместителем из-за преобладания положительного мезомерного эффекта над отрицательным индуктивным.
 В молекуле бензилового спирта гидроксильная группа не участвует в сопряжении и проявляет только отрицательный индуктивный эффект. Поэтому она является электроноакцепторным заместителем.
В молекуле бензилового спирта гидроксильная группа не участвует в сопряжении и проявляет только отрицательный индуктивный эффект. Поэтому она является электроноакцепторным заместителем.
Эти примеры показывают, что нельзя рассматривать влияние какого-либо заместителя вообще, а нужно рассматривать его влияние в конкретной молекуле.
 Только галогены всегда являются электроноакцепторными заместителями, т.к. их отрицательный индуктивный эффект проявляется сильнее, чем положительный мезомерный. Например:
Только галогены всегда являются электроноакцепторными заместителями, т.к. их отрицательный индуктивный эффект проявляется сильнее, чем положительный мезомерный. Например:

А теперь вернёмся к реакциям электрофильного замещения в производных бензола. Итак, мы выяснили, что заместитель, уже имеющийся в кольце, влияет на ход реакций электрофильного замещения. В чём же выражается это влияние?
Заместитель влияет на скорость реакций S E и на положение второго заместителя, вводимого в кольцо . Рассмотрим оба этих аспекта влияния.
Влияние на скорость реакции . Чем выше электронная плотность в кольце, тем легче протекают реакции электрофильного замещения. Понятно, что электронодонорные заместители облегчают реакции S E (являются активаторами цикла), а электроноакцепторные заместители – затрудняют их (дезактивируют цикл). Поэтому реакции электрофильного замещения в производных бензола, содержащих электроноакцепторные заместители, проводят в более жёстких условиях.
 Сравним активность фенола, толуола, бензола, хлорбензола и нитробензола в реакции нитрования.
Сравним активность фенола, толуола, бензола, хлорбензола и нитробензола в реакции нитрования.
Так как фенол и толуол содержат электронодонорные заместители, они более активны в реакциях S E , чем бензол. Наоборот, хлорбензол и нитробензол менее активны в этих реакциях, чем бензол, т.к. содержат электроноакцепторные заместители. Фенол активнее толуола из-за положительного мезомерного эффекта OH-группы. Хлор не такой сильный электроноакцепторный заместитель, как нитрогруппа, т.к. нитрогруппа проявляет и отрицательный индуктивный, и отрицательный мезомерный эффекты. Итак, в данном ряду активность в реакциях электрофильного замещения убывает от фенола к нитробензолу. Экспериментально установлено, что если скорость реакции нитрования бензола принять за 1, то этот ряд будет выглядеть так:
Вторым аспектом влияния заместителя в ароматическом кольце на ход реакций электрофильного замещения является так называемое ориентирующее действие заместителей . Все заместители можно подразделить на две группы: орто-, пара-ориентанты (заместители 1 рода) и мета-ориентанты (заместители 2 рода).
К заместителям 1 рода относятся: -OH, -O - , -NH 2 , алкильные группы (-CH 3 , -C 2 H 5 и т.д.) и галогены. Вы можете видеть, что все эти заместители проявляют положительный индуктивный эффект и (или) положительный мезомерный эффект. Все они, кроме галогенов, повышают электронную плотность в кольце, особенно в орто- и пара-положениях. Поэтому электрофил и направляется в эти положения. Рассмотрим это на примере фенола:
За счёт положительного мезомерного эффекта гидроксильной группы происходит перераспределение электронной плотности по сопряжённой системе, и в орто- и пара-положениях она особенно повышена.
 При бромировании фенола образуется смесь орто- и пара-бромфенола:
При бромировании фенола образуется смесь орто- и пара-бромфенола:
Если бромирование проводить в полярном растворителе (бромной водой) и использовать избыток брома, реакция протекает сразу по трём положениям:
 |
Заместителями 2 рода являются: -NH 3 + , -COOH, -CHO (альдегидная группа), -NO 2 , -SO 3 H. Все эти заместители понижают электронную плотность в ароматическом кольце, но из-за её перераспределения в мета-положениях она понижена не так сильно, как в орто- и пара-. Рассмотрим это на примере бензойной кислоты:
Карбоксильная группа проявляет отрицательный индуктивный и отрицательный мезомерный эффекты. За счёт перераспределения по сопряжённой системе в мета-положениях электронная плотность остаётся более высокой, чем в орто- и пара-, поэтому электрофил будет атаковать мета-положения:
 |
Первая группа реакций реакции замещения. Мы говорили, что арены не имеют кратных связей в структуре молекулы, а содержат сопряженную систему из шести электронов, которая очень стабильна и придает дополнительную прочность бензольному кольцу. Поэтому в химических реакциях происходит в первую очередь замещение атомов водорода, а не разрушение бензольного кольца.
С реакциями замещения мы уже сталкивались при разговоре об алканах , но для них эти реакции шли по радикальному механизму, а для аренов характерен ионный механизм реакций замещения.
Первое химическое свойство галогенирование. Замещение атома водорода на атом галогена хлора или брома.
Реакция идет при нагревании и обязательно с участием катализатора. В случае с хлором это может быть хлорид алюминия или хлорид железа три. Катализатор поляризует молекулу галогена, в результате чего происходит гетеролитический разрыв связи и получаются ионы.
Положительно заряженный ион хлора и вступает в реакцию с бензолом.
Если реакция происходит с бромом, то катализатором выступает бромид железа три или бромид алюминия.

Важно отметить, что реакция происходит с молекулярным бромом, а не с бромной водой. С бромной водой бензол не реагирует.
У галогенирования гомологов бензола есть свои особенности. В молекуле толуола метильная группа облегчает замещение в кольце, реакционная способность повышается, и реакция идет в более мягких условиях, то есть уже при комнатной температуре.
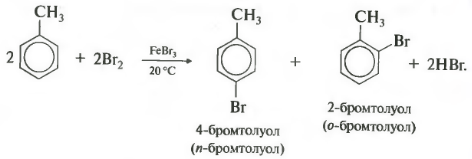
Важно отметить, что замещение всегда происходит в орто- и пара-положениях, поэтому получается смесь изомеров.
Второе свойство нитрование бензола, введение нитрогруппы в бензольное кольцо.

Образуется тяжелая желтоватая жидкость с запахом горького миндаля нитробензол, поэтому реакция может быть качественной на бензол. Для нитрования используется нитрующая смесь концентрированной азотной и серной кислот. Реакция проводится при нагревании.
Напомню, что для нитрования алканов в реакции Коновалова использовалась разбавленная азотная кислота без добавления серной.
При нитровании толуола, также как и при галогенировании, образуется смесь орто- и пара- изомеров.

Третье свойство алкилирование бензола галогеналканами.

Эта реакция позволяет ввести углеводородный радикал в бензольное кольцо и может считаться способом получения гомологов бензола. В качестве катализатора используется хлорид алюминия, способствующий распаду молекулы галогеналкана на ионы. Также необходимо нагревание.
Четвертое свойство алкилирование бензола алкенами.
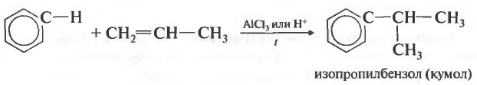
Таким способом можно получить, например, кумол или же этилбензол. Катализатор хлорид алюминия.
2. Реакции присоединения к бензолу
Вторая группа реакций реакции присоединения. Мы говорили, что эти реакции не характерны, но они возможны при достаточно жестких условиях с разрушением пи-электронного облака и образованием шести сигма-связей.
Пятое свойство в общем списке гидрирование, присоединение водорода.
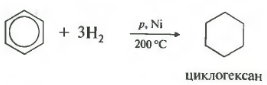
Температура, давление, катализатор никель или платина. Таким же образом способен реагировать толуол.
Шестое свойство хлорирование. Обратите внимание, что речь идет именно о взаимодействии с хлором, поскольку бром в эту реакцию не вступает.

Реакция протекает при жестком ультрафиолетовом облучении. Образуется гексахлорциклогексан, другое название гексахлоран, твердое вещество.
Важно помнить, что для бензола не возможны реакции присоединения галогеноводородов (гидрогалогенирование) и присоединение воды (гидратация).
3. Замещение в боковой цепи гомологов бензола
Третья группа реакций касается только гомологов бензола это замещение в боковой цепи.
Седьмое свойство в общем списке галогенирование по альфа-атому углерода в боковой цепи.

Реакция происходит при нагревании или облучении и всегда только по альфа-углероду. При продолжении галогенирования, второй атом галогена снова встанет в альфа-положение.
4. Окисление гомологов бензола
Четвертая группа реакций окисление.
Бензольное кольцо слишком прочное, поэтому бензол не окисляется перманганатом калия не обесцвечивает его раствор. Это очень важно помнить.
Зато гомологи бензола окисляются подкисленным раствором перманганата калия при нагревании. И это восьмое химическое свойство.

Получается бензойная кислота. Наблюдается обесцвечивание раствора. При этом, какой бы длинной не была углеродная цепь заместителя, всегда происходит ее разрыв после первого атома углерода и альфа-атом окисляется до карбоксильной группы с образованием бензойной кислоты. Оставшаяся часть молекулы окисляется до соответствующий кислоты или, если это только один атом углерода, до углекислого газа.
Если гомолог бензола имеет больше одного углеводородного заместителя у ароматического кольца, то окисление происходит по тем же правилам окисляется углерод, находящийся в альфа-положении.

В данном примере получается двухосновная ароматическая кислота, которая называется фталевая кислота.
Особым образом отмечу окисление кумола, изопропилбензола, кислородом воздуха в присутствии серной кислоты.

Это так называемый кумольный способ получения фенола. Как правило, сталкиваться с этой реакцией приходится в вопросах, касающихся получения фенола. Это промышленный способ.
Девятое свойство горение, полное окисление кислородом. Бензол и его гомологи сгорают до углекислого газа и воды.
Запишем уравнение горения бензола в общем виде.
По закону сохранения массы атомов слева должно быть столько же, сколько атомов справа. Потому что ведь в химических реакциях атомы никуда не деваются, а просто изменяется порядок связей между ними. Так вот молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле арена, поскольку в состав молекулы входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть (2n-6)/2, а значит n-3.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа, потому что в каждой молекуле два атома кислорода, плюс n-3 из воды, итого 3n-3. Слева атомов кислорода столько же 3n-3, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть (3n-3)/2 молекул кислорода.
Таким образом, мы составили уравнение сгорания гомологов бензола в общем виде.
Физические свойства
Бензол и его ближайшие гомологи – бесцветные жидкости со специфическим запахом. Ароматические углеводороды легче воды и в ней не растворяются, однако легко растворяются в органических растворителях – спирте, эфире, ацетоне.
Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ. Все арены горят коптящим пламенем ввиду высокого содержания углерода вих молекулах.
Физические свойства некоторых аренов представлены в таблице.
Таблица. Физические свойства некоторых аренов
|
Название |
Формула |
t°.пл., |
t°.кип., |
|
Бензол |
C 6 H 6 |
5,5 |
80,1 |
|
Толуол (метилбензол) |
С 6 Н 5 СH 3 |
95,0 |
110,6 |
|
Этилбензол |
С 6 Н 5 С 2 H 5 |
95,0 |
136,2 |
|
Ксилол (диметилбензол) |
С 6 Н 4 (СH 3) 2 |
||
|
орто- |
25,18 |
144,41 |
|
|
мета- |
47,87 |
139,10 |
|
|
пара- |
13,26 |
138,35 |
|
|
Пропилбензол |
С 6 Н 5 (CH 2) 2 CH 3 |
99,0 |
159,20 |
|
Кумол (изопропилбензол) |
C 6 H 5 CH(CH 3) 2 |
96,0 |
152,39 |
|
Стирол (винилбензол) |
С 6 Н 5 CH=СН 2 |
30,6 |
145,2 |
Бензол – легкокипящая ( t кип = 80,1°С), бесцветная жидкость, не растворяется в воде
Внимание! Бензол – яд, действует на почки, изменяет формулу крови (при длительном воздействии), может нарушать структуру хромосом.
Большинство ароматических углеводородов опасны для жизни, токсичны.
Получение аренов (бензола и его гомологов)
В лаборатории
1. Сплавление солей бензойной кислоты с твёрдыми щелочами
C 6 H 5 -COONa + NaOH t → C 6 H 6 + Na 2 CO 3
бензоат натрия
2. Реакция Вюрца-Фиттинга : (здесь Г – галоген)
С 6 H 5 -Г + 2 Na + R -Г → C 6 H 5 - R + 2 Na Г
С 6 H 5 -Cl + 2Na + CH 3 -Cl → C 6 H 5 -CH 3 + 2NaCl
В промышленности
- выделяют из нефти и угля методом фракционной перегонки, риформингом;
- из каменноугольной смолы и коксового газа
1. Дегидроциклизацией алканов с числом атомов углерода больше 6:
C 6 H 14 t , kat →C 6 H 6 + 4H 2
2. Тримеризация ацетилена (только для бензола) – р. Зелинского :
3С 2 H 2 600° C , акт. уголь →C 6 H 6
3. Дегидрированием циклогексана и его гомологов:
Советский академик Николай Дмитриевич Зелинский установил, что бензол образуется из циклогексана (дегидрирование циклоалканов
C 6 H 12 t, kat →C 6 H 6 + 3H 2

C 6 H 11 -CH 3 t , kat →C 6 H 5 -CH 3 + 3H 2
метилциклогексантолуол
4. Алкилирование бензола (получение гомологов бензола) – р Фриделя-Крафтса .
C 6 H 6 + C 2 H 5 -Cl t, AlCl3 →C 6 H 5 -C 2 H 5 + HCl
хлорэтан этилбензол

Химические свойства аренов
I . РЕАКЦИИ ОКИСЛЕНИЯ
1. Горение (коптящее пламя):
2C 6 H 6 + 15O 2 t →12CO 2 + 6H 2 O + Q
2. Бензол при обычных условиях не обесцвечивает бромную воду и водный раствор марганцовки
3. Гомологи бензола окисляются перманганатом калия (обесцвечивают марганцовку):
А) в кислой среде до бензойной кислоты
При действии на гомологи бензола перманганата калия и других сильных окислителей боковые цепи окисляются. Какой бы сложной ни была цепь заместителя, она разрушается, за исключением a -атома углерода, который окисляется в карбоксильную группу.
Гомологи бензола с одной боковой цепью дают бензойную кислоту:
Гомологи, содержащие две боковые цепи, дают двухосновные кислоты:
5C 6 H 5 -C 2 H 5 + 12KMnO 4 + 18H 2 SO 4 → 5C 6 H 5 COOH + 5CO 2 + 6K 2 SO 4 + 12MnSO 4 +28H 2 O
5C 6 H 5 -CH 3 + 6KMnO 4 + 9H 2 SO 4 → 5C 6 H 5 COOH + 3K 2 SO 4 + 6MnSO 4 +14H 2 O
Упрощённо:
C 6 H 5 -CH 3 + 3O KMnO4 →C 6 H 5 COOH + H 2 O
Б) в нейтральной и слабощелочной до солей бензойной кислоты
C 6 H 5 -CH 3 + 2KMnO 4 → C 6 H 5 COO К + K ОН + 2MnO 2 + H 2 O
II . РЕАКЦИИ ПРИСОЕДИНЕНИЯ (труднее, чем у алкенов)
1. Галогенирование
C 6 H 6 +3Cl 2 h ν → C 6 H 6 Cl 6 (гексахлорциклогексан - гексахлоран)
2. Гидрирование
C 6 H 6 + 3H 2 t , Pt или Ni →C 6 H 12 (циклогексан)
3. Полимеризация
III . РЕАКЦИИ ЗАМЕЩЕНИЯ – ионный механизм(легче, чем у алканов)
б) гомологов бензола при облучении или нагревании
По химическим свойствам алкильные радикалы подобны алканам. Атомы водорода в них замещаются на галоген по свободно-радикальному механизму. Поэтому в отсутствие катализатора при нагревании или УФ-облучении идет радикальная реакция замещения в боковой цепи. Влияние бензольного кольца на алкильные заместители приводит к тому, что замещается всегда атом водорода у атома углерода, непосредственно связанного с бензольным кольцом (a -атома углерода).
1) C 6 H 5 -CH 3 + Cl 2 h ν → C 6 H 5 -CH 2 -Cl + HCl
в) гомологов бензола в присутствии катализатора
C 6 H 5 -CH 3 + Cl 2 AlCl 3 → (смесь орта, пара производных) +HCl
2. Нитрование (с азотной кислотой)
C 6 H 6 + HO-NO 2 t, H2SO4 →C 6 H 5 -NO 2 + H 2 O
нитробензол - запах миндаля !
C 6 H 5 -CH 3 + 3HO-NO 2 t, H2SO4 → С H 3 -C 6 H 2 (NO 2) 3 + 3H 2 O2,4,6-тринитротолуол (тол, тротил)
Применение бензола и его гомологов
Бензол C 6 H 6 – хороший растворитель. Бензол в качестве добавки улучшает качество моторного топлива. Служит сырьем для получения многих ароматических органических соединений – нитробензола C 6 H 5 NO 2 (растворитель, из него получают анилин), хлорбензола C 6 H 5 Cl, фенола C 6 H 5 OH, стирола и т.д.
Толуол C 6 H 5 –CH 3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ).
Ксилолы C 6 H 4 (CH 3) 2 . Технический ксилол – смесь трех изомеров (орто -, мета - и пара -ксилолов) – применяется в качестве растворителя и исходного продукта для синтеза многих органических соединений.
Изопропилбензол C 6 H 5 –CH(CH 3) 2 служит для получения фенола и ацетона.
Хлорпроизводные бензола используют для защиты растений. Так, продукт замещения в бензоле атомов Н атомами хлора – гексахлорбензол С 6 Сl 6 – фунгицид; его применяют для сухого протравливания семян пшеницы и ржи против твердой головни. Продукт присоединения хлора к бензолу – гексахлорциклогексан (гексахлоран) С 6 Н 6 Сl 6 – инсектицид; его используют для борьбы с вредными насекомыми. Упомянутые вещества относятся к пестицидам – химическим средствам борьбы с микроорганизмами, растениями и животными.
Стирол C 6 H 5 – CH = CH 2 очень легко полимеризуется, образуя полистирол, а сополимеризуясь с бутадиеном – бутадиенстирольные каучуки.
ВИДЕО-ОПЫТЫ
По химическим свойствам бензол и другие ароматические углеводороды отличаются от предельных и непредельных углеводородов. Наиболее характерны для них реакции замещения атомов водорода бензольного ядра. Они протекают легче, чем у предельных углеводородов. Таким путем получают множество органических соединений. Так, при взаимодействии бензола с бромом (в присутствии катализатора FеВr 2) атом водорода замещается атомом брома:
При другом катализаторе можно все атомы водорода в бензоле заместить на галоген. Это происходит, например, при пропускании в бензол хлора в присутствии хлорида алюминия:
Если на бензол действовать смесью концентрированных азотной и серной кислот (нитрующей смесью), то атом водорода замещается нитрогруппой - NО 2:
Это реакция нитрования бензола. Нитробензол - бледно-желтая маслянистая жидкость с запахом горького миндаля, нерастворима в воде, применяется в качестве растворителя, а также для получения анилина.
В молекуле бензола можно заместить атом водорода на алкильный радикал действием галогенопроизводных углеводородов в присутствии хлорида алюминия:
Реакции присоединения к бензолу протекают с большим трудом. Для их протекания необходимы особые условия: повышение температуры и давления, подбор катализатора, световое облучение и др. Так, в присутствии катализатора - никеля или платины - бензол гидрируется, т.е. присоединяет водород, образуя циклогексан:
Циклогексан – бесцветная летучая жидкость с запахом бензина, в воде нерастворим.
При ультрафиолетовом облучении бензол присоединяет хлор:
Гексахлорциклогексан, или гексахлоран, - кристаллическое вещество, применяется как сильное средство для уничтожения насекомых.
Бензол не присоединяет галогеноводороды и воду. Он очень устойчив к окислителям. В отличие от непредельных углеводородов он не обесцвечивает бромную воду и раствор KMnO 4 . В обычных условиях бензольное кольцо не разрушается и при действии многих других окислителей. Однако гомологи бензола подвергаются окислению легче предельных углеводородов. При этом окислению подвергаются лишьрадикалы, связанные с бензольным кольцом:
Таким образом, ароматические углеводороды могут вступать как в реакции замещения, так и в реакции присоединения, однако условия этих превращений значительно отличаются от аналогичных превращений предельных и непредельных углеводородов.
Получение. Бензол и его гомологи в больших количествах получают из нефти и каменноугольной смолы, образующейся при сухой перегонке каменного угля (коксовании). Сухая перегонка производится на коксохимических и газовых заводах.
Реакция превращения циклогексана в бензол (дегидрогенизация или дегидрирование) протекает при пропускании его над катализатором (платиновой чернью) при 300°С. Предельные углеводороды реакцией дегидрогенизации также можно превращать в ароматические. Например:
Реакции дегидрирования позволяют использовать углеводороды нефти для получения углеводородов ряда бензола. Они указывают на связь между различными группами углеводородов и на взаимное превращение их друг в друга.
По способу Н.Д. Зелинского и Б.А. Казанского бензол можно получить, пропуская ацетилен через нагретую до 600° С трубку с активированным углем. Весь процесс полимеризации трех молекул ацетилена можно изобразить схемой
Реакции электрофильного замещения - реакции замещения, в которых атаку осуществляет электрофил - частица, заряженная положительно или имеющая дефицит электронов. При образовании новой связи уходящая частица - электрофуг отщепляется без своей электронной пары. Самой популярной уходящей группой является протон H + .
Все электрофилы являются кислотами Льюиса.
Общий вид реакций электрофильного замещения:
(катионный электрофил)
(нейтральный электрофил)
Механизм реакции S E Ar или реакции ароматического электрофильного замещения является самым распространенным и наиболее важным среди реакций замещения ароматических соединений и состоит из двух стадий. На первом этапе происходит присоединение электрофила, на втором - отщепление электрофуга:
В ходе реакции образуется промежуточный положительно заряженный интермедиат (на рисунке - 2b). Он носит название интермедиат Уэланда , арониевый ион или σ-комплекс . Этот комплекс, как правило, очень реакционноспособен и легко стабилизируется, быстро отщепляя катион.
